Révolution ces 10 dernières années !
Même si les biothérapies ont fortement contribué à cette évolution, il est bon de rappeler certains points importants de cette dernière décennie concernant les arthrites juvéniles idiopathiques (AJI).
Quest-ce que les AJI en 2011 ?
Les arthrites juvéniles idiopathiques ont été mieux classifiées ces dix dernières années avec les critères de Durban en 1997 revisités à Edmonton en 2001. Comme on peut le voir ces critères ont tout juste 10 ans ! Et au moment de lécriture de cet article, de nouveaux critères viennent encore dêtre publiés.
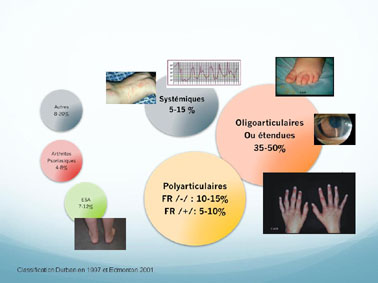
Arthrites de cause inconnue survenant chez les enfants de moins de 16 ans et dune durée de plus de 6 semaines, les AJI se distinguent en 7 types darthrites différentes :
les arthrites dites systémiques,
les oligoarthrites qui peuvent rester oligoarticulaires ou devenir après 6 mois dévolution étendue,
les polyarthrites à facteur rhumatoïde positif et
les polyarthrites à facteur rhumatoïde négatif,
les arthrites associées aux enthèsites (inflammation des insertions tendineuses),
les arthrites psoriasiques et
les arthrites non classées.
Chacune de ces arthrites a une définition qui lui est propre et elle diffère des autres par son mode de présentation, les anomalies observées dans la prise de sang, lâge auquel survient la maladie, les manifestations extra-articulaires (comme les uvéites dans les formes oligoarticulaires ou la fièvre et latteinte cutanée dans les formes systémiques par exemple), par son pronostic à plus ou moins long terme ou encore par le traitement qui devra être prescrit.
En effet, on sait à ce jour que certains médicaments seront plus adaptés pour certaines et non pour dautres. La recherche scientifique a permis de comprendre que ces arthrites peuvent être différentes entre elles par les facteurs cellulaires ou les cytokines qui jouent un rôle principal dans la maladie et qui pourraient conduire dans le futur à la prescription de thérapies plus ciblées.
Concept de pluridisciplinarité pour la prise en charge des AJI ?
La prise en charge des enfants atteints dAJI a également progressé avec le concept de pluridisciplinarité. Durant ces dernières années, la collaboration étroite de pédiatres et de rhumatologues a permis de traiter les petits patients le plus rapidement possible mais également de tenir compte des problèmes à plus long terme que ces patients peuvent rencontrer : comme les troubles de la croissance, lostéoporose, les troubles de fertilité
Les connaissances, les compétences et les expériences de chacun ont nettement amélioré la prise en charge des enfants, des adolescents ou des jeunes adultes. Des programmes et des consultations de « translation » adolescents-adultes se sont aussi mises en place pour assurer le suivi des patients. Laide de kinésithérapeutes, dassistants sociaux ou de psychologue est un atout supplémentaire pour accompagner les soins médicaux et améliorer la prise en charge.
Des centres dits de référence en rhumatologie pédiatrique se sont également développés. Même sil sagit encore de pathologies rares (1enfant sur 2.000), il est essentiel que ce soit des médecins formés et compétents qui soccupent de ces pathologies.
Evaluation de la maladie et échelle de qualité de vie !
De nombreux travaux ont été réalisés pour valider des échelles ou des scores qui permettent comme chez les adultes dévaluer la répercussion fonctionnelle de la maladie sur le quotidien des petits patients. Etablies au départ (comme lACR pedi) sur des scores dactivité de la maladie chez les adultes (ACR), dautres échelles se
sont élaborées et adaptées aux problèmes propres aux enfants (CHAQ, JADAS
).
Ces échelles permettent dune part de connaître lactivité de la maladie à un moment donné mais également de déterminer lefficacité dun traitement.
Enfin, le développement de registre de patients est un outil considérable pour mieux connaître cette maladie ainsi que les problèmes qui peuvent y être liés. Ces registres permettent dencoder toutes les données des patients atteints dAJI, les maladies associées, les traitements pris ou en cours, les effets secondaires qui peuvent être liés à la maladie ou aux traitements.
Ainsi, ils peuvent être une source intéressante pour la recherche génétique ou scientifique. Depuis un an, en Belgique, nous avons ouvert un registre pour les AJI sans et sous biothérapies.
Quel traitement pour quel patient ?
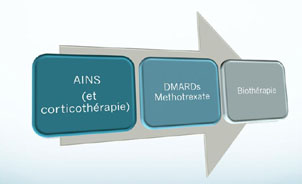
Le traitement des AJI débute le plus souvent par la prescription danti-inflammatoires non stéroïdiens et la majorité des AJI ne nécessiteront pas dautres médicaments. Ce sont les formes oligoarticulaires qui répondent le mieux à ces molécules.
Les formes plus sévères ou polyarticulaires auront parfois besoin dun traitement dit de fond (appelé aussi DMARDs) supplémentaire dont le plus efficace de nos jours est le méthotrexate, administré oralement ou sous forme intramusculaire ou en sous-cutanée de manière hebdomadaire qui suffit souvent à contrôler efficacement la maladie.
La prescription de cortisone est parfois utilisée pour contrôler des poussées inflammatoires ou les formes systémiques plus sévères. Enfin pour les formes plus graves ou mal contrôlées par ces trois types de traitement, on devra prescrire des biothérapies.
Même si plusieurs biothérapies sont actuellement souvent utilisées chez les adultes, en Belgique nous ne disposons que de letanercept (enbrel) comme biothérapie remboursée chez les enfants.
Il sagit dun agent bloquant le TNF sous la forme dun faux récepteur dit soluble qui capte le TNF circulant lempêchant de se fixer sur sa cible. Cette molécule est disponible depuis 2002 et est indiquée dans les AJI chez des enfants dâge ≥ 2 ans qui présentent plus de 5 articulations inflammatoires réfractaires au MTX ainsi que de linflammation dans le sang mesurée par la CRP.
Administré en sous-cutané, dabord deux fois par semaine ( 2002 à 2008) (0 ,4 mg/kg), on le prescrit depuis 3 ans à raison dune fois par semaine (0,8mg/kg).
Dans dautres pays cependant, comme aux USA, dautres biothérapies sont autorisées par la FDA (Food Drug Administration) et prescrites depuis 2008 pour les AJI, comme ladalimumab ( AJI ≥ 4ans) et labatacept ( AJI ≥ 6 ans et réfractaire à un anti-TNF). Ces molécules ne sont pas encore autorisées en Belgique mais le seront bientôt.
Par contre linfliximab (autre anti-TNF), disponible pour traiter les adultes atteints de polyarthrite rhumatoïde, de spondylarthrite ankylosante ou de rhumatisme psoriasique, na reçu lautorisation américaine en 2006 que pour la maladie de Crohn juvénile (maladie inflammatoire chronique du tube digestif) et non pour lAJI.
Les biothérapies sont-elles efficaces dans l AJI ?
Bien que les études cliniques soient difficiles à réaliser chez les enfants selon les modalités habituelles et du fait du petit nombre denfants sévèrement atteints, les anti-TNF et principalement letanercept et ladalimumab ont montré une efficacité chez plus de 75% des enfants traités.
Une étude récente montre que, à 8 ans de traitement, 100% des enfants considérés comme répondeurs au traitement sont toujours sous ce même médicament. Certains enfants ont arrêté ce traitement soit par manque defficacité, soit parce que la maladie semblait suffisamment contrôlée et considérée pour être en rémission.
Plusieurs études ont également montré que les formes qui répondaient le moins bien aux anti-TNF étaient les formes systémiques.
Dautre part, il a été démontré que la combinaison des anti-TNF et du méthotrexate était meilleure quen monothérapie. Outre leffet positif sur la maladie (amélioration des douleurs, des gonflements articulaires et des activités quotidiennes des enfants), une amélioration des troubles de la croissance (en effet lAJI peut se compliquer par une petite taille si elle nest pas traitée) a été observée sous anti-TNF liée en partie par le contrôle de la maladie inflammatoire et en partie par la réduction de la corticothérapie.
Quels sont les effets secondaires des biothérapies dans lAJI ?
De manière globale les anti-TNF dans larthrite juvénile sont bien tolérés. A lexception dinfections plus fréquentes, relativement peu deffets secondaires ont été observés. Il est à rappeler que les biothérapies comme le methotrexate sont contre-indiquées en cas dadministration concomitante de vaccins vivants tels que les vaccins contre la rougeole, oreillons, rubéole, varicelle, poliomyélite oral ou fièvre jaune. Il faut dès lors tenir compte de cette contre-indication lors de la mise en route de ces traitements chez les enfants.
Et le risque de cancer ?
En 2009, la FDA (organisme américain du contrôle des médicaments) a tiré la sonnette dalarme sur un risque possible de cancers (principalement du sang comme les lymphomes) associés aux biothérapies chez les enfants.
Mais cela a été démenti par les études et les résultats obtenus dans les différents registres (doù limportance des données que peuvent nous apporter ces registres). Même si on a pu démontrer que le risque de cancer de manière générale était moindre chez les enfants que chez les adultes, les cas de lymphomes rapportés chez les enfants traités par anti-TNF étaient surtout des cas observés chez des enfants atteints de maladie de Crohn liée probablement à la maladie elle-même et à la prise simultanée dImuran® (lazathioprine = un immunosuppresseur prescrit dans cette pathologie inflammatoire des intestins) mais non liée à lAJI elle-même.
En conclusion, on peut dire aujourdhui que les anti-TNF naugmentent pas le risque de cancers chez nos petits patients. Même sil faut rester prudent, nous pouvons à ce jour être rassurés sur ce point.

Et demain ?
Même si à ce jour, nous ne disposons officiellement que dune seule biothérapie pour traiter les enfants atteints darthrite juvénile, nous avons de belles perspectives pour traiter les petits patients qui ne répondent pas à cette molécule.
Nous pouvons dans certains centres de référence disposer soit dautres anti-TNF comme ladalimumab, soit dune autre biothérapie comme labatacept (molécule qui bloque la communication entre des cellules de linflammation) et ce pour les formes dites polyarticulaires. Bientôt remboursées par la mutuelle, elles sont disponibles dans le cadre de « programme à usage médical » mais restent réservées pour des formes sévères et seulement dans des centres de référence.
Pour les formes dites systémiques, plus sévères, souvent corticodépendantes et répondant moins bien aux anti-TNF, nous pouvons disposer de molécules bloquant linterleukine-6 (une autre molécule de linflammation particulièrement impliquée dans ces formes), le tocilizumab mais toujours dans le cadre de ce type de programme car non remboursées à ce jour.
Enfin, dans les formes systémiques, il existe une autre molécule de linflammation pouvant être bloquée par une biothérapie, linterleukine-1. Mais cette fois, son blocage par un anticorps, le canakinumab, ne peut être prescrit que dans le cadre de protocole thérapeutique. Néanmoins, lensemble de ces « futurs » traitements nous permet de voir lavenir sous de meilleurs cieux, denvisager de meilleures perspectives de prise en charge et de pronostic des AJI.
Projets dans le futur ?
Des projets de recherche scientifique se tournent maintenant sur une meilleure identification des différentes formes dAJI et des molécules impliquées dans la maladie, sur le dépistage de marqueurs pronostics de la maladie et de marqueurs de réponse aux différents traitements (permettant didentifier les bons ou les mauvais répondeurs avant la mise en route des différents traitements), de même que sur la disponibilité de données épidémiologiques, médicales et de suivi des patients atteints dAJI, par les registres par exemple.
En espérant quil faudra moins des dix prochaines années pour obtenir ces résultats
Dr Valérie Badot
Membre du comité scientifique
|